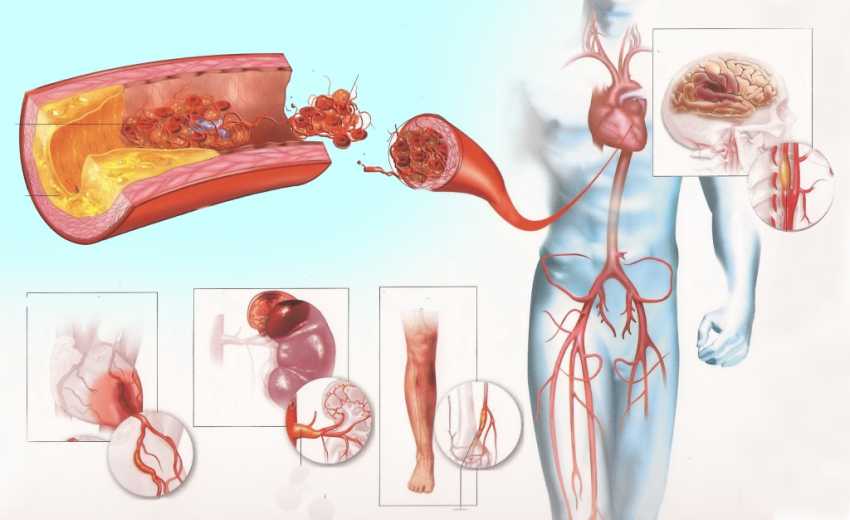
Ишемическая болезнь сердца. ИБС – симптомы, причины и лечение
Ишемическая болезнь сердца, по определению Всемирной организации здравоохранения, представляет собой острую или хроническую дисфункцию сердца, возникшую вследствие абсолютного или относительного уменьшения снабжения миокарда артериальной кровью.
«Медицина как комплекс научных знаний и практических методов по сохранению и укреплению здоровья человека, профилактике заболеваний и лечению заболевших является основой социального института, именуемого здравоохранением».
Существующей догмой в формировании «доказательной базы» выступает «скрининг» (буквально – «просеивание»), т.е. – контролируемое исследование, по сути – эксперимент. В зависимости от цели, его необходимым условием является выявление факторов риска (ФР) болезней среди практически здорового населения, предикторов прогрессирования болезни, а также анализ и практическая реализация методов их предупреждения.
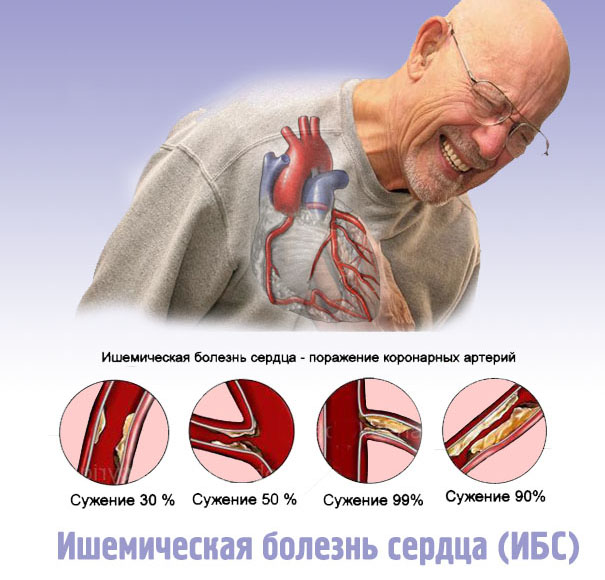
В настоящее время ВОЗ развивает международную систему мониторирования ФР. Первичная профилактика сердечно-сосудистых заболеваний (ССЗ) предполагает использование шкал риска для выявления групп высокого риска и назначения профилактических вмешательств. Однако, это сопряжено с необходимостью тщательной оценки данных. Фремингемская шкала менее эффективна, чем нагрузочные (спироэргометрия) пробы и Европейская шкала сердечно-сосудистого риска (SCORE), которые позволяют оценивать риск смерти от ССЗ даже у асимптомных пациентов.
Безусловно, приоритетным направлением лечения ишемической болезни сердца (ИБС) является улучшение выживаемости больных за счет уменьшения числа новых случаев инфаркта миокарда и внезапной сердечной смерти.
Известно, что монотерапия одним из антиангинальных препаратов гемодинамического действия в большинстве случаев оказывается недостаточно эффективной. На практике широко применяются комбинации двух или трех антиангинальных препаратов. Например, в многоцентровом исследовании, проводившемся в США, в котором участвовали 1266 врачей общей практики и 5125 пациентов, частота назначения комбинаций антиангинальных препаратов составила 65%. По данным российской части многоцентрового исследования Angina Treatment Pattern (ATP), в котором участвовали 167 врачей из 17 регионов России, набравших 1653 пациента, частота назначения комбинированной терапии достигла 76%. Естественно, назначая комбинацию препаратов, врачи ожидают существенного увеличения антиангинальной эффективности такой терапии. Однако данные ряда многоцентровых исследований свидетельствуют скорее об обратном.
Иследования ишемической болезни сердца
Так, в исследовании TIBET комбинированное лечение БАБ и АК не превосходило по эффективности монотерапию каждым из препаратов в отдельности. В исследовании IMAGE был отмечен некоторый благоприятный эффект комбинированной терапии, однако подчеркивалось, что он был обусловлен действием другого препарата, а не собственно комбинации.
W.Klein и соавт. 2006 провели мета-анализ 22 рандомизированных исследований, в которых, по результатам нагрузочных проб, сравнивалась эффективность монотерапии БАБ или АК с эффективностью их комбинации. Мета-анализ показал, что комбинированная терапия приводит к возрастанию общей продолжительности нагрузки, времени до появления депрессии сегмента ST на 1 мм и времени до развития приступа стенокардии (на 5,8 и 12% соответственно) в сравнении с монотерапией БАБ и только времени до появления депрессии сегмента ST на 1 мм (на 9%) в сравнении с монотерапией АК. Важно, что данные различия были достоверными только в первые 6 часов приема комбинации препаратов.
По данным российской части исследования ATP, несмотря на проводимую комбинированную антиангинальную терапию, у 64% больных с ИБС высокого ФК сохранялось более 5 приступов стенокардии в неделю. При этом резко возрастает число побочных эффектов лечения (риск полипрагмазии).
В связи с этим в Европейских рекомендациях по лечению стабильной стенокардии прямо указывается, что перед назначением комбинации антиангинальных препаратов необходимо оценить эффект монотерапии препаратом другого класса.
Таким образом, необходимость усиления эффективности медикаментозных подходов существует.
Цитопротекторная терапия
Термин «цитопротекция» подразумевает осмысление эндогенных механизмов защиты. Дискредитации этой идеи в последнее время способствовала ограниченная клиническая база существующих средств, а также отсутствие их в арсенале зарубежных коллег, что традиционно рассматривается как признак нашей ущербности. Но именно зарубежные коллеги впервые доказали эффективность метаболической стратегии с позиции «доказательной медицины». И это, по мнению А.Н.Пархоменко (2008), способствовало кристаллизации современных представлений о метаболической терапии, а точнее – метаболической кардиопротекции. По определению R.Ferrari (1999),
«Цитопротекторная терапия – это то лечение, которое путем прямого влияния на кардиомиоцит способствует его выживаемости в условиях ишемии (гипоксии)».
Подобные взгляды были сформулированы еще в конце 60-х – начале 70-х годов прошлого столетия. Один из основателей концепции «контроля» ишемического повреждения E. Braunwald в 1974 году писал: «Я верю, что мы сейчас находимся на пороге новой эры в лечении острого инфаркта миокарда. Теперь можно вполне обоснованно полагать, что миокардиальная ткань вовсе не обречена на гибель только потому, что она лежит в зоне васкуляризации коронарной артерии, подвергшейся обструкции». Таким образом, сформировалось четкое представление о том, что объем ишемического повреждения миокарда в виде некроза может быть уменьшен, в частности, с помощью фармакологических средств, стимулирующих гликолиз.
Алгоритм медикаментозной терапии стабильной стенокардии. Рекомендации ЕОК, 2006 г.
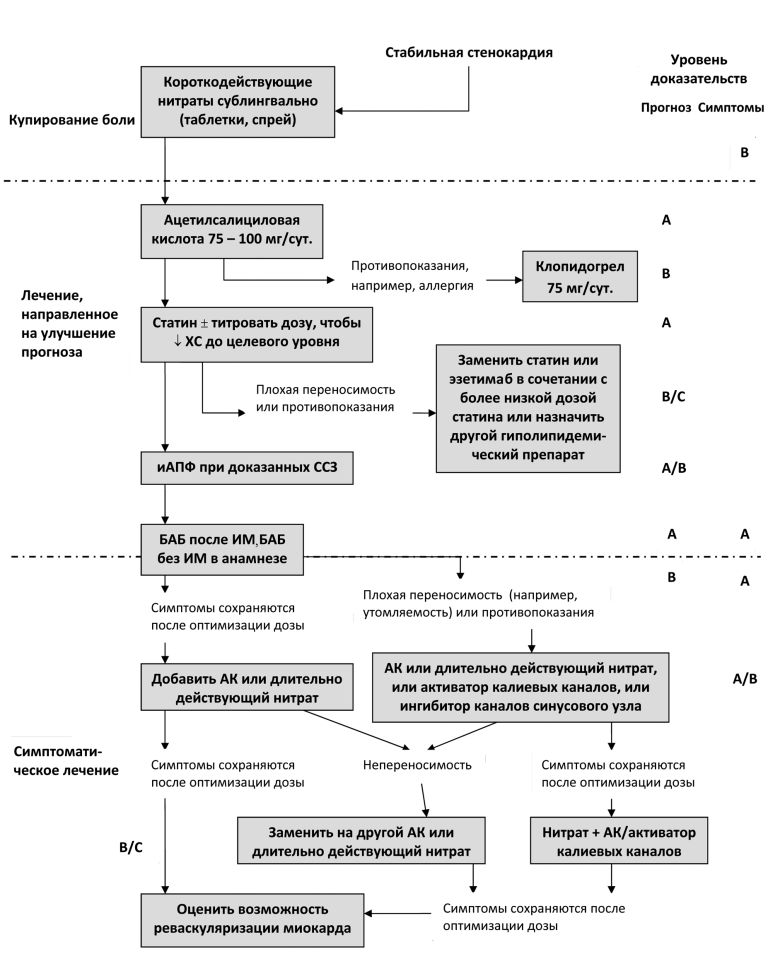
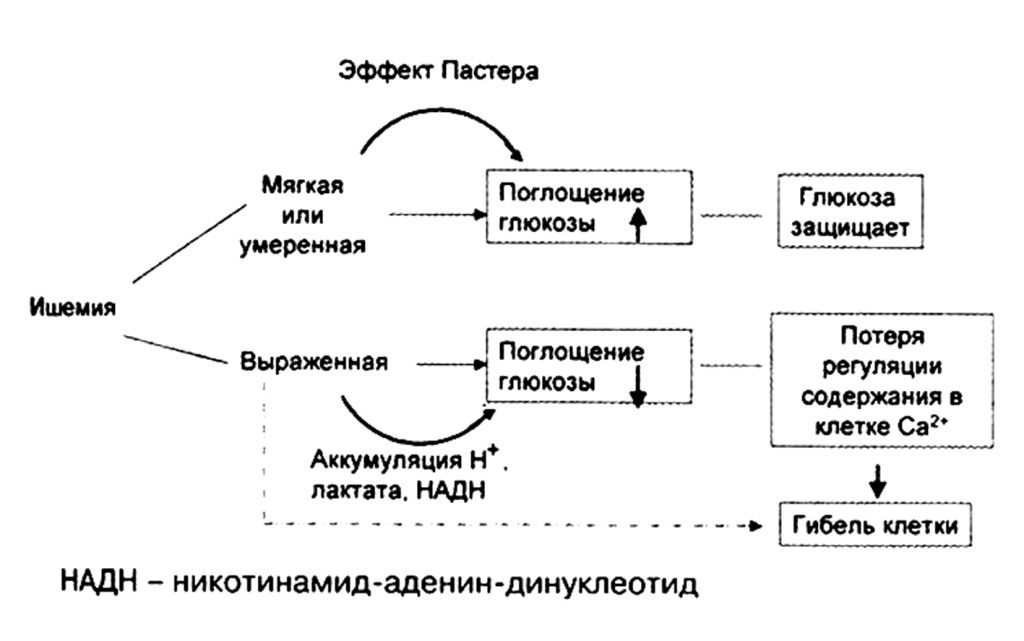 Хорошо известный триметазидин блокирует один из этапов окисления жирных кислот и способствует, по реципрокному механизму, впервые описанному Randel (1967), компенсаторному усилению окисления глюкозы. Следует подчеркнуть, что это не единственный положительный эффект триметазидина: его цитопротекторные свойства могут быть связаны с его способностью ускорять синтез фосфоиназитидов и активизировать обмен фосфолипидов в клетках миокарда, что было установлено в работах A. Grynberg (2001). Хотя остается непонятным, почему триметазидин при внутривенном введении не улучшает состояния больных с инфарктом миокарда (EMIR-FR, 1997).
Хорошо известный триметазидин блокирует один из этапов окисления жирных кислот и способствует, по реципрокному механизму, впервые описанному Randel (1967), компенсаторному усилению окисления глюкозы. Следует подчеркнуть, что это не единственный положительный эффект триметазидина: его цитопротекторные свойства могут быть связаны с его способностью ускорять синтез фосфоиназитидов и активизировать обмен фосфолипидов в клетках миокарда, что было установлено в работах A. Grynberg (2001). Хотя остается непонятным, почему триметазидин при внутривенном введении не улучшает состояния больных с инфарктом миокарда (EMIR-FR, 1997).
Подобный подход реализован в препарате ранолазин, который является парциальным ингибитором окисления жирных кислот. Его эффективность в качестве антиишемического средства подтверждена крупными исследованиями MARISA и CARISA. Ранолазин в состоянии оказывать дополнительное антиишемическое действие в случае достижения максимальных доз АК.
Перспективность ранолазина представляется весомой, поскольку препарат легко проникает в митохондрии, но вызывает только частичное (т.е. только во время ишемии) блокирование свободных жирных кислот, не мешая их окислению после устранения ишемического эпизода.
Несомненный интерес представляет собой попытка влиять на энергетику митохондрий посредством стимуляции окисления глюкозы в ишемизированной клетке и не блокировать окисление жирных кислот в условиях нормоксии. Это достигается посредством стимуляции пентозофосфатного пути окисления глюкозы. Этот подход реализован в механизме действия комбинированного препарата ритмокор, содержащим как основное действующее вещество глюконовую кислоту, а также ионы магния и калия. Глюконовая кислота является аллостерическим модулятором реакций пентозного шунта, который в энергетическом смысле не зависит от наличия кислорода. Особенно велика активность шунта в проводящей системе сердца. Вероятно, именно поэтому препарат обладает способностью устранять нарушения ритма сердца ишемического генеза. Возможно, в этом большую роль играет наличие в препарате магния в самой биодоступной форме.
По данным мета-анализа 9 проведенных ранее исследований (25000 человек), высокое содержание магния в пище снижает риск диабета на 23%. Данные другого мета-анализа (286668 человек и 10000 случаев заболевания) показали, что включение в рацион дополнительного приема препаратов магния с высокой биодоступностью способствует снижению риска сахарного диабета, который, как известно, важнейший предиктор (ФР) смерти от ССЗ. В то же время данные мета-анализа (18000 человек) свидетельствуют не только о снижении риска заболевания, но и улучшении течения уже существующего диабета – уменьшению инсулинорезистентности и метаболического синдрома. Таким образом, возможность влияния как на предиктор болезни, так и на патогенетический механизм ее развития, является стратегической.
В отношении магниевой терапии можно сказать о его патогенетической значимости не только при сахарном диабете, но и при артериальной гипертонии (STOP-hypertension DASH), где установлено, что применение магния, а еще в большей степени калия снижает как систолическое, так и диастолическое артериальное давление, причем независимо от уровня калиемии или магниемии. Последние молекулярные исследования установили, что внутриклеточная гипомагнигистия (которая, кстати, встречается почти в 50%, по крайней мере, в американском регионе; у нас информация отсутствует), вызванная дефектом в системе каналов-переносчиков, является стимулом пролиферации фибробластов и ответственна за развитие болезней, ассоциированных с возрастом.
Как показали результаты последних мета-анализов, это справедливо в отношении уровня С-реактивного белка, холестерина и липопротеидов низкой плотности, прогноза при метаболическом синдроме и сахарном диабете, т.е. магниевая терапия может быть эффективной стратегией модификации факторов риска и безопасного этиологического влияния на них.
Кроме того, как показало Framinghem Heart Study, длительная гипомагниемия коррелирует с высокой частотой возникновения нарушений сердечного ритма (желудочковых экстрасистол, тахикардии, фибрилляции желудочков), а при оценке результатов PROMISE Study сделано заключение о большей частоте желудочковой экстрасистолии и высокой летальности в группе больных с гипомагниемией при сравнении с группами, в которых отмечалась нормо- и гипермагниемия. Еще более неожиданными оказались результаты мета-анализов, посвященных эффективности и безопасности магниевой терапии при фибрилляции предсердий – успешный контроль частоты желудочкового ответа, особенно в сочетании с гликозидной терапией, а также модуляция эффективности препаратов 3 класса (ибутилида и амиодарона) при стратегии восстановления синусового ритма.
По данным исследования о значении уровней магнезиемии и калиемии в развитии и прогрессировании сердечной недостаточности установлено, что в расчете на 10000 человеко/лет смертность от сердечно-сосудистой патологии (прогрессирование СН) в группе пациентов с низким или низко-нормальным уровнем калия и магния достоверно была выше (p=0,024), а от всех причин – приближалась к уровню достоверности (p=0,06), но не влияла на количество госпитализаций.
Все вышеизложенное заставляет произвести переосмысление существующих догм и подчеркивает перспективность нового направления в терапии сердечно-сосудистых заболеваний – применение препаратов с полипотентным влиянием на факторы риска и патогенез болезни.
Однако существуют и другие подходы к цитокардиопротекции, и они связаны с расширением наших познаний об эволюционных процессах защиты клеток. Особенно это справедливо после установления роли митохондрий в реализации, пожалуй, самого важного кардиопротекторного механизма, названного прекондиционированием.
Феномен прекондиционирования заключается в существенном повышении устойчивости миокарда к ишемическому и реперфузионному повреждению, возникающему после нескольких коротких эпизодов ишемии/реперфузии. В экспериментальных исследованиях показана значительная инфарктлимитирующая и антиаритмическая эффективность прекондиционирования, а также его способность ослаблять постишемическую сократительную и эндотелиальную дисфункцию. Этот защитный феномен был идентифицирован R.A. Kloner и D. Yellon (1994 г.) и в клинической практике.
Процесс прекондиционирования протекает в две стадии: ранняя (во время которой запускаетcя каскадный медиаторный механизм, приводя к развитию ишемического прекондиционирования) и поздняя – «второе окно защиты» – повышает толерантность в отношении летальной ишемии миокарда через 24 часа длительностью до 72 часов. В механизмы развития защитного эффекта ишемического прекондиционирования вовлечено множество различных факторов, среди которых значение имеет модулирующее влияние системы, генерирующей NO, и связанной с этим активации синтезов белков теплового шока (HSP – heat shock protein), но согласно последним сведениям, ведущую роль играют митохондриальные (и в меньшей мере сарколеммальные) АТФ-зависимые К+-каналы и активация А1-рецептора аденозина, поскольку инфузия аденозина полностью воспроизводит защитный эффект прекондиционирования.
Имеются многочисленные доказательства, что фармакологическое открытие АТФ-зависимых К+-каналов полностью воспроизводят защитный эффект ишемического прекондиционирования, а их блокада, наоборот, способствует ухудшению течения ИБС. Впервые этот эффект описал A.Noma в 1983 г. В 2002 году Y.P.Wang с коллегами представили убедительные данные, свидетельствующие о кардиопотективном действии в фазе позднего прекондиционирования повышении продукции NO посредством стимулирования выработки ее синтазы (Inducible Syntase NO – iNOS). Известно, индуцированная изоформа NO синтазы содержится во многих клетках организма, в частности, в кардиомиоцитах, гладкомышечных клетках сосудов, макрофагах.
В этой связи заслуживают внимания результаты исследования Impact of Nicorandil in Angina, 2001 (IONA), поскольку посвящены препарату, сочетающему в себе свойства донатора NO и активатора К+-каналов – никорандилу. В исследование IONA вошли 5126 пациентов со стабильной стенокардией и высоким риском неблагоприятных исходов. Никорандил существенно (на 17%) снизил риск наступления первичной конечной точки – в основном за счет уменьшения частоты острых коронарных синдромов без развития ИМ (на 21%) и общего количества сердечно-сосудистых осложнений (14%). Общая смертность на фоне лечения никорандилом достоверно не изменилась, хотя была отмечена тенденция к ее снижению (на 15%). Из побочных эффектов при приеме никорандила отмечена головная боль.
Поскольку, как уже упоминалось, в развитии эффектов прекондиционирования значительная роль отводится не только активаторам митохондриальных каналов, но и мессенджерам, связанным с активацией сарколемальных калиевых каналов. К таким мессенджерам относится аденозин, активирующий пуриновые рецепторы.
Экспериментальными работами показано, что применение аденозина вызывает феномен ишемического прекондиционирования, оказывает ингибирующее действие на миграцию нейтрофилов, высвобождение цитокинов из мононуклеаров, уменьшает продукцию кислородных радикалов и частоту апоптоза. Кроме того, аденозин проявляет антитромбоцитарный эффект, способствуя улучшению проходимости коронарной артерии и микроциркуляторной перфузии.
В пилотном исследовании Acute Myocardial Infarction Study of Adenosine (AMISTAD-I, 1999 г.) при тромболитической терапии (ТЛТ), выполненной у 236 больных ИМ, отмечено достоверное 33% уменьшение размеров некроза после 3-часовой инфузии аденозина в дозе 70 мкг/кг/мин в сравнении с контролем. Тем не менее, этот эффект был недостаточен для улучшения клинических исходов и обнаружен только при передней локализации инфаркта.
Исследование AMISTAD-II (2005) было организовано как крупное многоцентровое двойное-слепое плацебо-контролируемое исследование по оценке эффективности аденозина в дополнение к реперфузионным вмешательствам у больных ИМ с подъемом сегмента ST.
Исследование AMISTAD-II подтвердило, что использование аденозина в дозе 70 мкг/кг/мин в дополнение к реперфузионной терапии значительно (на 57%) уменьшает размеры ИМ. Однако в оценке клинических конечных точек отмечен лишь слабый тренд в сторону улучшения, что, по мнению авторов, связано с недостаточным объемом исследования.
Лечение ИБС, препарат адвокард
Недостатком естественного активатора А1 рецепторов – аденозина следует считать неудобство применения, связанное с необходимостью внутривенного введения через инфузомат под тщательным контролем показателей гемодинамики, а также быстрой деградацией препарата в кровеносном русле. Поэтому перспективным направлением является создание веществ, подобных аденозину, но имеющих благоприятный фармакокинетический профиль. Именно такой является субстанция магладена – аденозин-трифосфато-Mg (II)-глюконат, входящая в состав комбинированного препарата Адвокард® . В состав Адвокарда® входит молсидомин, который выступает в роли модулятора (а не донатора) эффектов NO, связанных со стимуляцией процессов прекондиционирования активацией аденозиновых рецепторов магладеном. Таким образом, Адвокард® проявляет, в первую очередь, свойство цитопротектора, а уже во-вторых – оказывает положительное влияние на показатели системной гемодинамики: стимуляция пуриновых рецепторов сопровождается дилатацией мелких артериол, а молсидомин расширяет вены среднего диаметра, поэтому такое потенциирование является гемодинамически выгодным для организма.
По результатам исследований, Адвокард® оказывает антиишемическое действие, улучшает метаболизм миокарда. Применение препарата у больных ИБС со стабильной стенокардией напряжения II-III ФК показало его безопасность и эффективность: уменьшение эпизодов ишемии миокарда по результатам суточного мониторирования ЭКГ по Холтеру.
Прием Адвокарда® у пациентов с ИБС со стабильной стенокардией напряжения II ФК оказывает достоверное положительное влияние на клиническое течение симптомов ИБС и толерантность к физической нагрузке по сравнению с плацебо.
О.В.Коркушко с соавт. (2008) установили, что препарат достоверно увеличивает толерантность к физической нагрузке в сравнении с плацебо.
Представляют интерес данные, полученные С.А.Андриевской с соавт. (2008) о положительном влиянии Адвокарда® на безболевую ишемию миокарда ББИМ. Назначение Адвокарда® приводит к изменениям в структуре ишемического эпизода в сторону явного уменьшения безболевых форм под влиянием терапии с включением активатора аденозиновых рецепторов. Это свидетельствует о возможном регулирующем влиянии Адвокарда® на ноцицептивную составляющую регуляции сердечной деятельности.
Таким образом, активаторы калиевых каналов сегодня представляют реально существующий класс средств, механизм которых связан со стимуляцией адаптивных процессов в клетке, способствующих защите от повреждения, поэтому их в прямом смысле следует считать цитокардиопротекторами. Именно в связи с их уникальными кардиопротекторными свойствами в рекомендации Рабочей группы Европейского общества кардиологов по ведению больных стабильной стенокардией (2006) в качестве базисной терапии введен класс активаторов калиевых каналов.
Вадим КОЗЛОВСКИЙ, Валентин ШМАЛИЙ, Олег КОЛЕСНИК, Ольга ТЕР-САРКИСОВА, Олег КОЗЛОВСКИЙ
Научный центр «ФАРКОС»
Винницкий национальный медицинский университет им. Н.И.Пирогова
Житомирский областной центр медико-социальной экспертизы