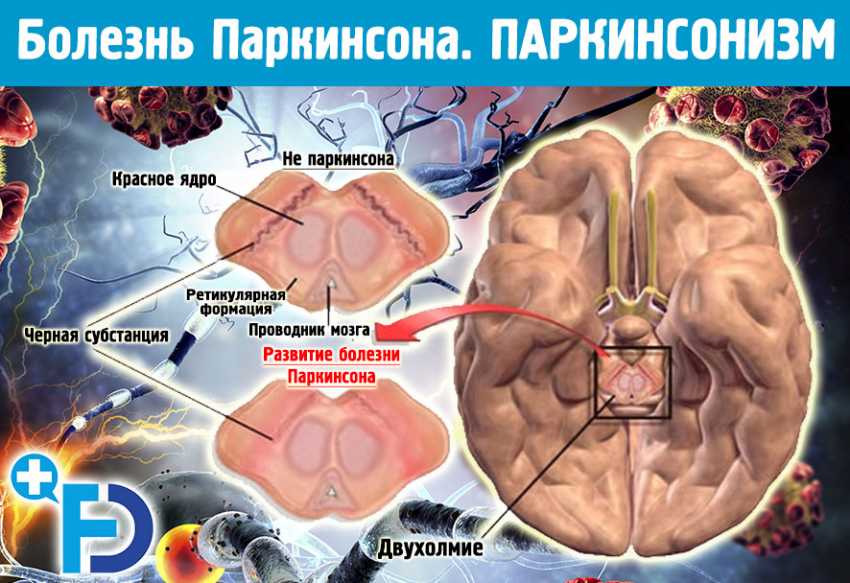
ПАРКИНСОНИЗМ. Болезнь Пакринсона: причины, симптомы и лечение
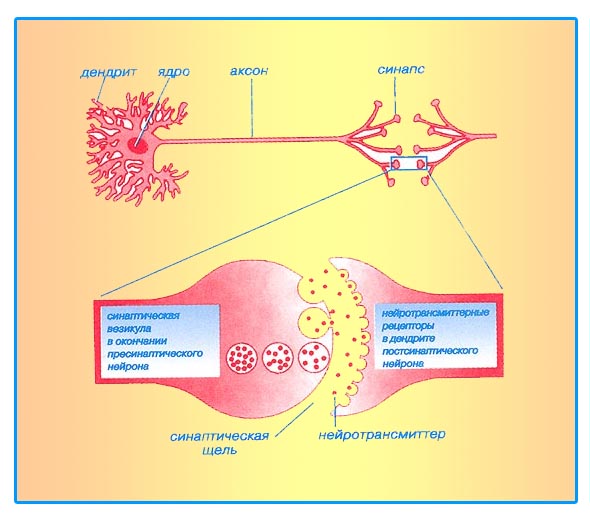
Болезнь паркинсона (гипертонично–гипокинетический синдром, палидарний синдром) – синдром экстрапирамидных расстройств с преимущественным поражением палидуму, где основными симптомами являются гипокинезия, повышение мышечного тонуса, тремор покоя, постуральные расстройства.
 Этот синдром может быть осложнением целого ряда патологий – черепно – мозговых травм, сосудисто – мозговых расстройств, эпидемического энцефалита Экономо, отравлений марганцем, цианидами, окисью углерода, а также быть одним из основных или дополнительных проявлений многих наследственных нейродегенеративных заболеваний.
Этот синдром может быть осложнением целого ряда патологий – черепно – мозговых травм, сосудисто – мозговых расстройств, эпидемического энцефалита Экономо, отравлений марганцем, цианидами, окисью углерода, а также быть одним из основных или дополнительных проявлений многих наследственных нейродегенеративных заболеваний.
Среди случаев синдрома паркинсонизма, обусловленных признанными причинами, выделяют болезнь Паркинсона (первичный, идиопатический паркинсонизм, дрожащий паралич) – хроническое прогрессирующее нейродегенеративное заболевание нервной системы, где причинно – следственная связь с каким-то фактором не выявлено, считается, что болезнь имеет наследственный характер, хотя четкая наследственная линия не всегда проявляется. Болезнь паркинсона проявляется характерными двигательными расстройствами в виде акинезии, тремора и мышечной ригидности, к которым в дальнейшем могут присоединяться нарушения вегетативной регуляции, когнитивных функций, эмоциональной сферы.
Патогенетическая основа паркинсонизма
В основе дрожащего паралича, или болезни Паркинсона, заключаются дегенеративные изменения с потерей меланин – вмистних нейронов черной субстанции и дофаминергических нейронов стриатума – дегенерация наследственно предопределена.
В случае других причин клинического синдрома говорится о паркинсонизм, или паркинсоноподобных синдром, что отражено в классификации (по J.Jankovic, 1994), где представлены статистические показатели встречаемости патологии и причинно – следственные связи с тем или иным патогенным фактором.
Классификация паркинсонизма и частота встречаемости отдельных его форм
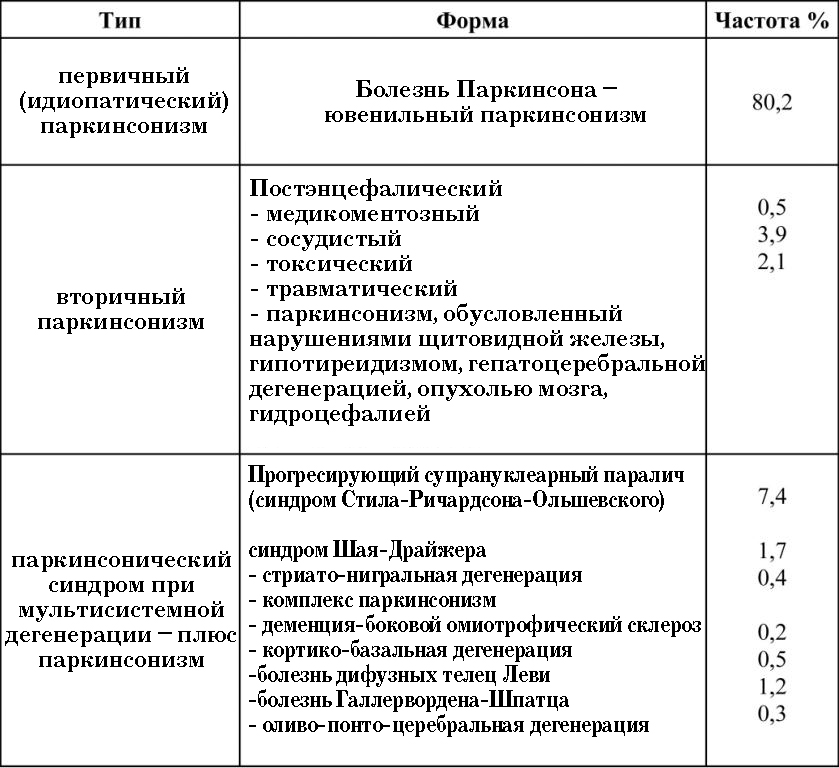
Как видно из таблицы, именно болезнь Паркинсона встречается чаще: БП составляет 75–80 % случаев среди проявлений паркинсонизма. Заболевание распространено на всей планете, и частота его не зависит от расы и существенно увеличивается с возрастом, колеблясь по разным данным в диапазоне 60–140 случаев на 100 000 населения. Клинически болезнь обычно начинается в возрасте около 55–60 лет, редко заболевание может развиться в возрасте до 40 лет (паркинсонизм с ранним началом) или до 20 лет (ювенильный паркинсонизм). В возрастной группе старше 60 лет, больные составляют 1 %, а в популяции более 85 лет – 2,6 %. Среди заболевших преобладают мужчины.
Как отмечалось, этиология БП до сих пор окончательно не выяснена. Вместе с тем присутствие большого спектра доказанных факторов риска (старение, генетическая предрасположенность, влияние факторов окружающей среды и т.д.) отображает мультифакториальной природу патологии.
Согласно статистике, как отмечалось, зустричаемисть БП коррелирует с более старшим возрастом – старением. И известно, что патоморфологический нормальное старение сопровождается уменьшением количества нейронов черной субстанции и наличием в них телец Леви, а также нейрохимическими изменениями в стриатуме – снижением содержания дофамина и фермента тирозингидроксилазы наряду с уменьшением количества дофаминовых рецепторов. За то, с помощью ПЭТ было доказано в несколько раз выше темпы дегенерации нейронов черной субстанции при БП в отличие от нормального старения.
Патоморфология, патогенез. На основании морфологических исследований, К. Третьяков в 1919 году предположил, что причиной паркинсонизма является поражение черной субстанции. Эта гипотеза затем была многократно подтверждена другими исследователями. Основу всех форм паркинсонизма составляет резкий спад дофамина в черной субстанции и полосатом теле.
Исследование «взаимоотношений» между черной субстанцией и полосатым телом показали, что они имеют двусторонний характер и работают по принципу обратной связи. Влияние хвостатого ядра на черную субстанцию происходит с помощью ГАМК, а также других нейротрансмиттеров. Стриарные гамкергични нейроны, влияя на активность дофаминергических нейронов черной субстанции, тем самым контролируют уровень дофамина в полосатом теле. Хвостатое ядро, кроме тормозных влияний, может осуществлять на черную субстанцию и возбуждающее влияние с помощью субстанции Р. Нейроны, содержащие этот медиатор, проектируются с хвостатого ядра в черную субстанцию. Таким образом, нигростриарни связи является сложной функциональной системой, не однородна по своим физиологическим и биохимическим компонентами, поэтому самые нарушения в этой системе и окружающих ее образованиях приводят к развитию основных клинических симптомов паркинсонизма.
Симптомы болезни паркинсона
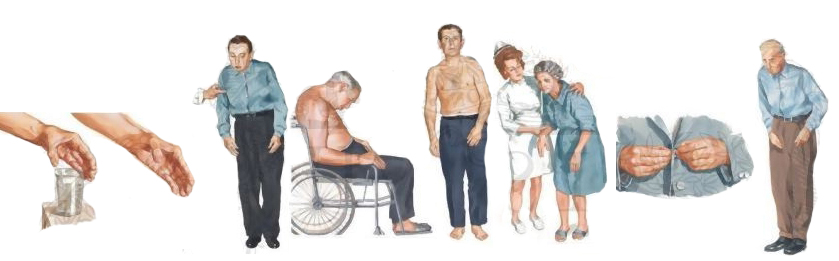
Гипокинезия, ригидность, тремор, постуральные расстройства.
Для установления диагноза паркинсонизма должны быть, как минимум, два из четырех названных выше симптомов.
В развернутых типичных случаях паркинсонизма могут прослеживаться варианты указанных симптомов:
• Олигокинезия, брадикинезия, акинезия.
• «Шаркая» (старческая) походка мелкими шагами, вне « просителя », « сгибателей ».
Нарушение мимики – гипомимия, тоническая фиксация мимических реакций.
• Брадикинезия взгляда, жидкое моргания.
• Медленная, тихая, монотонная, маломодульована речь.
• Экстрапирамидная мышечная ригидность, феномен «зубчатого колеса» (симптом Негро).
• Тремор покоя (головы, нижней челюсти, в кистях – «счета монет»).
• Потеря физиологических синкинезий.
• Пропульсия. Симптом «воздушной подушки».
• Психоэмоциональные расстройства ( патологическая навязчивость – акайрия, аспонтанность т.п.).
• Вегетативные расстройства (жирная себорея, запоры и др.).
Гипокинезия и Брадикинезия
Гипокинезия проявляется трудностями инициации произвольных, спонтанных и автоматизированных движений. У больного при попытке начать движение предназначенные для этого мышцы – агонисты сокращаются недостаточно, что делает движение слишком медленным, и он часто не достигает конечной цели. Одним из вариантов гипокинезии является брадикинезия.
Брадикинезия – замедление движений с прогрессивным уменьшением амплитуды при их повторном выполнении. Первыми проявлениями могут быть затруднения и неудобство мелких движений пальцев – застегивания пуговиц, завязывание шнурков, перелистывания книги, должно не остаться без внимания семейного врача. Как проявления гипокинезии – уменьшение амплитуды физиологической синкинезии – расшатывание рук при ходьбе ( ахейрокинез ), укорочение шага ( шаркая походка), обеднение мимических движений ( гипомимия ). Лицо становится маскообразным, выражая иногда застывшую гримасу удивления или сумму, которая может быть связано с некоторым расширением глазных щелей. Значительно уменьшаются мигательные движения век, речь становится монотонной и невнятной. Часто мимика не успевает изменяться согласно тематике событий ( разговора), что вызывает у собеседников подозрение относительно неадекватности партнера по общению. При гипокинезии особенно затрудняется одновременное выполнение различных движений, а также комплексных движений. Внимательное наблюдение за больным семейным врачом позволяет выявить все эти признаки, несмотря на то, что сначала они бывают выражены незначительно, часто только на одной половине тела ( гемипаркинсонизма ) и / или в дистальных группах мышц. Впоследствии они втягивают множество мышечных групп билатерально, отображающий прогрессирующий характер патологии.
Гипокинезия является наиболее инвалидизирующих признаком болезни паркинсона!
Клиническая верификация гипокинезии в дебюте паркинсонизма в практике врача общей практики несложная и содержит несколько проб:
• Ритмичное быстрое постукивание большим и указательным пальцами ;
• Постукивание ногой по полу ;
• Пронация – супинация рук;
• Изучение почерка пациента (выявление микрографии ).
Тяжелым проявлением акинезии является так называемый феномен «застывания» – резкое и неожиданное полное прекращение двигательной активности. Больные могут длительное время поддерживать позы, невозможные для здоровых людей, например лежать, держа голову над подушкой (симптом «воздушной подушки »). Чаще всего « застывания » возникают при попытке встать со стула, начать ходьбу, вернуться или пройти через узкое пространство – дверной проем, коридор. Остановиться больному порой бывает так же трудно, как и начать движение. Изредка наблюдается феномен « парадоксальной кинезии »: больной, тяжело встает со стула, может легко выбегать лестнице, ходить, переступая через небольшие препятствия, танцевать. Временное « растормаживания », как правило, провоцируется аффектами радости или страха. При идиопатической БП феномен «застывания» обычно наблюдается на поздних стадиях и, возможно, является осложнением длительной терапии дофаминергическими препаратами. Интересно, что при других нейродегенеративных заболеваниях (прогрессирующий надъядерный паралич) феномен « застывания », преимущественно в виде нарушения инициации ходьбы, может иметь место уже в самом начале болезни.
Патофизиологические механизмы гипокинезии остаются до конца невыясненными. Вероятно, что возникновение гипокинезии является результатом нарушения связей между базальными ганглиями, премоторной и моторной корой.
Ригидность что это?
Ригидность – повышение тонуса мышц, ощущаемая больным и определяется объективно врачом во время пассивных движений в суставе, и обусловлено одновременным сокращением мышц агонистов и антагонистов. Ригидность часто бывает асимметричной, особенно в начале заболевания. Она наиболее выражена в сгибателях конечностей и аксиальных мышцах. Степень ригидности может варьироваться в течение дня, может увеличиваться при стрессах и уменьшаться после сна и отдыха.
Ригидность мышц часто бывает причиной боли в спине и плечевом суставе, реже – пояснице. Такие болевые синдромы могут быть первыми признаками паркинсонизма и нередко приводят к неправильным диагнозов. Поэтому такие симптомы, когда больной жалуется на постоянные изнуряющие боли в плечевом поясе и спине, мало зависят от физических нагрузок и, особенно, если сопровождаются хотя бы малейшими проявлениями гипокинезии, беспричинным снижением настроения, должны вызывать настороженность семейного врача, особенно, если в семье ' й случаи паркинсонизма. Клиническую оценку состояния мышечного тонуса, который вызывает сомнения у врача при обычном осмотре, и выявления асимметрии, позволяют повести несложные специальные приемы – попросить пациента делать движения контралатеральной рукой или сжать ее в кулак. При этом тонус на исследуемом стороне увеличивается. При ригидности мышц во время пассивного движения исследователь чувствует одинаковое сопротивление на протяжении всего движения как при сгибании, так и при разгибании ( симптом « свинцовой трубки» ).
Степень сопротивления в отличие от спастичности практически не зависит от скорости движения или от усилий. Если при исследовании ригидности отмечается периодическое увеличение сопротивления, создает впечатление соскакивания зубов, как бы цепляются между собой ( шестерня ), свидетельствует о феномене « зубчатого колеса », который обусловлен тремором, что наслаивается на ригидность.
Прогрессирование заболевания сопровождается постепенным ростом ригидности, что проявляется развитием характерной позы с функциональным доминированием сгибателей: председатель согнута и наклонена вперед, руки согнуты в локтевых суставах и прислоненный к туловищу, спина согнута, ноги слегка согнуты в тазобедренных и коленных суставах.
Что такое тремор покоя?
Тремор покоя – типичный симптом БП – идиопатического паркинсонизма. При других паркинсонических синдромах тремор или отсутствует вовсе, или имеет характер постурального или кинетического тремора. Амплитуда тремора увеличивается при умственной нагрузке, стрессе, при движении конечностями, не вовлеченных в тремор (например, амплитуда тремора в руках усиливается при ходьбе), и уменьшается при произвольном движении той конечности, вовлечена в тремор. Во время сна паркинсонический тремор исчезает. Частота типичного тремора покоя составляет около 4–8 Гц. Частота дрожания в разных частях тела может быть различной, что свидетельствует об отсутствии единого генератора паркинсонизма ритма. Он варьирует по интенсивности в течение дня, исчезая во время сна. Примерно у 75% больных с БП тремор является первым проявлением болезни и может быть легко замечен при осмотре пациента. Наиболее типичные ритмические движения большого пальца кисти в направлении других, напоминающие счет монет или скатывание пилюль. Иногда больные жалуются на ощущение дрожания внутри себя. Тремор начинается обычно в дистальной части одной конечности ( чаще в руке) и очень редко в ноге. В ногах тремор покоя проявляется, когда больной лежит или сидит, но, как правило, исчезает в положении стоя и при ходьбе. По мере прогрессирования болезни тремор распространяется на проксимальные участки руки, затем на ипсилатеральную ногу и на контралатеральной руку. Позже возможно привлечение подбородок или губ. Выраженность тремора может уменьшаться при значительном повышения ригидности на поздних стадиях заболевания вплоть до полного его исчезновения. В 30–60 % из БП наряду с тремором покоя может проявляться постуральный и кинетический тремор.
Постуральная неустойчивость
Постуральная неустойчивость (ПН) – это снижение или отсутствие способности поддержания положения центра тяжести тела, в сочетании с акинезией и ригидностью приводит к нарушению ходьбы и падения. ПН предпочтительно развивается через несколько лет от начала заболевания и становится инвалидизирующих на поздних стадиях болезни. Вследствие выраженной гипокинезии затрудняется инициация изменение движений. Когда больной начинает ходьбу или хочет изменить ее направление, возникает впечатление, что он начинает топтаться на месте, все больше наклоняясь вперед. На самом деле он пытается « догнать» центр тяжести тела мелкими шагами ( пропульсия ). Нередко это может закончиться падением, при этом больные не способны предупредить ушибы, так как защитная реакция – упор на руки – в них не успевает срабатывать. В отличие от мозжечковой атаксии, больные не расставляют широко ноги при ходьбе при паркинсонизме.
Для объективного выявления постуральной неустойчивости врач должен попросить пациента стоять, соединив стопы вместе, а за спиной больного неожиданно, но несильно, потянуть его за плечи назад. Пациенты с нарушенными постуральными рефлексами сделают более два шага назад для того, чтобы удержаться в вертикальном положении ( ретропульсия ). При более грубых нарушениях больной может упасть. Нарушение равновесия сопровождения – верждаемой замедленностью и неадекватностью предупредительных постуральных реакций в случае угрозы падения. Вероятно, что патогенез этих расстройств обусловлен нарушением модулирующих влияний бледного шара на участки премоторной коры, тесно связан с подготовкой и координацией движения.
Как вариант нарушения контроля над мышечным тонусом и содружеством движений довольно часто у больных возникают расстройства конвергенции и аккомодации, реже – блефароспазм.
Нарушение вегетативных функций
Нарушение вегетативных функций – еще один признак паркинсонизма. У большинства больных отмечается: гиперсаливация, сальность кожи лица, повышение потливости или, наоборот, сухость кожи, задержка мочеиспускания. Больные часто жалуются на запоры, обусловленные атонией толстой кишки. Могут возникать вегетативные кризы, сопровождающиеся резкой гиперемией лица, повышенной потливостью, тахикардией, эмоциональным напряжением, страхом.
Типичными для пациентов, больным паркинсолнизм, психические расстройства, такие, как когнитивные нарушения вплоть до деменции, депрессия, состояние спутанности и даже психозы. Врач должен помнить, что они могут быть связаны не только с самой болезнью, но и индуктуватися противопаркинсоническими препаратами или быть проявлением сопутствующего психического заболевания. Также может встречаться сочетание этих факторов у одного больного, существенно осложняет ситуацию. Поэтому в каждом конкретном случае врач должен проводить тщательное исследование.
Преимущественно встречаются легкие когнитивные нарушения, не достигающие степени деменции. Деменция встречается примерно в 10–25 % больных уже на поздних стадиях болезни. Не исключено, что сопутствующая синильная деменция альцгеймеривского типа является причиной более высокой частоты деменции в летней популяции больных БП по сравнению с более молодым контингентом. Другой формой, при которой характерно сочетание синдрома паркинсонизма и слабоумия, является деменция с тельцами Леви, может быть зплутана с болезнью Альцгеймера.
Депрессия при паркинсонизме
Депрессия легкой или средней степени встречается в большей части больных БП. Нередко она имеет место у больных уже на начальных стадиях заболевания, иногда предшествует проявлению двигательного дефекта и может храниться на фоне успешной терапевтической коррекции двигательных расстройств. В части случаев носит реактивный характер в ответ на тяжелый двигательный дефект или усиливается органично обусловленными причинами. С другой стороны, есть много свидетельств в пользу того, что депрессия при БП являются результатом органического поражения мозга. Навязчивость ( « акайрия » ), что в прошлом считалась неотъемлемой чертой БП, реально встречается не так уж часто.
У большинства больных БП наблюдаются нарушения сна в виде затрудненного засыпания, уменьшение продолжительности сна и его фазы с быстрыми движениями глаз. Расстройства сна часто связаны с ночной акинезией – трудностями поворотов во сне. Такие пациенты также жалуются на частые ночные пробуждения, после которых они долго не могут уснуть.
Сенсорные симптомы (боль, жжение, похолодание, онемение и другие ) наблюдаются почти у половины пациентов с БП, и часто является поводом для ошибочной диагностики суставно –мышечных или других заболеваний.
Инструментальные исследования, в том числе и МРТ, не могут подтвердить диагноз БП и проводятся только для исключения других заболеваний, приведенных выше. Только позитронно – эмиссионная томография позволяет подтвердить диагноз, даже на доклинической стадии, путем выявления снижения накопления радиоактивного препарата флуородопы в полосатом теле.
Соотношение выраженности основных симптомов заболевания у разных больных может значительно колебаться. В связи с этим различают акинетико – ригидную, ригидно – дрожащую и трепетную формы. Определение формы заболевания является весьма существенным фактором при выборе метода лечения.
Лечение паркинсонизма, лечение болезни паркинсона
Лечение паркинсонизма. Исходя из того, что степень выраженности симптомов БП прямо связана с уровнем дофамина в нигростриарний системе головного мозга, с этим связан и выбор лекарственных препаратов для лечения БП.
На начальной стадии заболевания дефицит дофамина выражен минимально, несмотря на дегенерацию значительной части клеток черной субстанции. Сохранены клетки способны обеспечить адекватный уровень дофамина за счет увеличения синтеза и выделения дофамина в единицу времени. Эта стадия БП может считаться частично компенсированной, следовательно, для лечения оптимальными являются препараты, нормализующие дофаминовый обмен. Кроме того, необходимые лекарства, способные замедлить дегенерацию нейронов и прогрессирование болезни, следовательно, нужны препараты, имеющие нейропротекторный эффект.
По мере развития болезни паркинсона возникает выраженный дефицит дофамина и наступает декомпенсированная стадия заболевания. Задача терапии на этой стадии – обеспечить необходимый уровень дофаминергической активности или путем назначения леводопы, как предшественник дофамина, или путем непосредственной стимуляции дофаминовых рецепторов их агонистами. Таким образом, в современной стратегии лечения БП принято выделять три этапа: 1 – лечение начальных стадий заболевания, в том числе нейропротекцию 2 – лечение развернутой БП 3 – лечения поздних стадий БП и борьба с осложнениями длительной дофаминергической терапии.
Алгоритм лечения БОЛЕЗНИ ПАРКИНСОНА
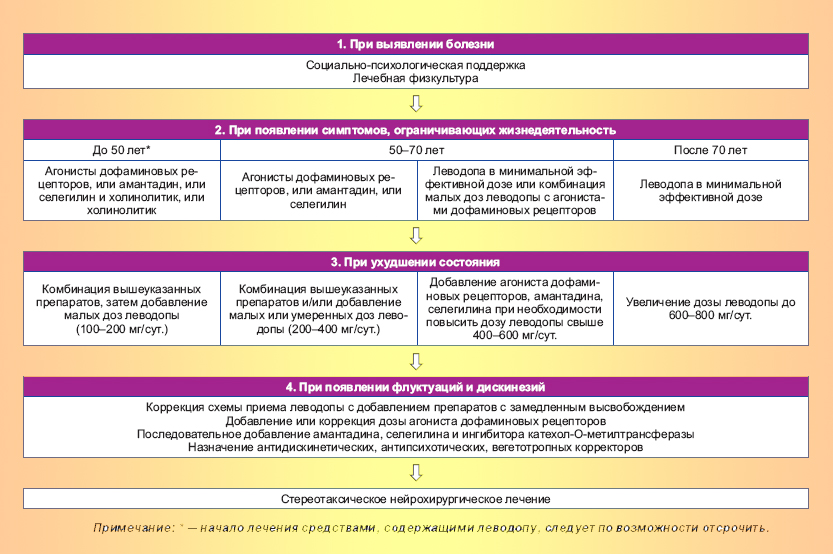
Лечение начальных стадий болезни паркинсона
Лечебная программа каждого пациента должна быть индивидуализирована с учетом выраженности отдельных симптомов заболевания, степени функциональной дезадаптации, а также наличия побочных эффектов терапии. Не следует стремиться к полной ликвидации симптомов заболевания.
Задача леченияболезни паркинсона – добиться восстановления повседневной активности больного минимально возможных дозах лекарственных препаратов. При мягких симптомах с минимальной дезадаптацией больного ( например, легкий тремор в одной руке) симптоматическая лекарственная терапия может не назначаться. В этом случае пациент должен сохранять достаточную физическую активность и периодически наблюдаться у врача. Если же возникают ригидность, гипокинезия или тремор, затрудняющих выполнение бытовой или профессиональной деятельности, то необходимо назначение медикаментозной терапии.
Конечно, адекватным принципом лечения является восстановление нарушенного баланса нейротрансмиттеров, что имеет выражение в:
• Или в повышении уровня дофамина в мозге ;
• Или снижении уровня ацетилхолина.
Кроме того, большое значение имеет нейропротекция.
Стратегия терапевтического воздействия на метаболизм дофамина при паркинсонизме
Увеличение синтеза дофамина
• Прекурсоры дофамина: леводопа / ингибитор дофадекарбоксилазы ( мадопар, синемет, наком ) ;
• Направленное воздействие на фармакодинамику леводопы ( синемет –С, мадопар ГСС, диета с соблюдением белкового баланса) ;
• Регуляция синтеза тирозингидроксилазы ( NADH – инфузии).
Стимуляция выброса дофамина из гранул сохранения в пресинаптической части дофаминового синапса:
• Блокаторы глутаматных рецепторов ( амантадин, мемантин ) ;
• Агонисты дофамина ( бромокриптин, перголид, ропинерол, апоморфин и др.)..
Торможение процесса обратного захвата дофамина:
• Антихолинергические средства ( паркопан, бипериден, тригексифенидил т.п.);
• Трициклические антидепрессанты ( амитриптилин ).
Торможение процесса катаболизма дофамина:
• Ингибиторы МАО –В ( селегилин ) ;
• Ингибиторы КОМТ ( толкапон, энтакапон ).
Нейропротекция дофаминовых нейронов:
• Антиоксиданты ( селегилин, токоферол, аскорбиновая кислота) ;
• Блокаторы кальциевых каналов (нифедипин ) ;
• Геропротекторы – цитомедины ( тималин, эпиталамин ).
Выбор препарата для начала медикаментозной терапии определяется возрастом больного, формой заболевания и уровнем необходимой функциональной активности больного.
Что должен знать врач общей практики
1). При подозрении паркинсонизмом согласно выявленным жалобами врач должен провести неврологический осмотр с применением клинических проб и учетом диагностических критериев, указанных выше. Следует помнить, что у пациента могут быть и другие патологии, симптоматика которых наслаивается на проявления экстрапирамидных расстройств и усиливает их, поэтому применение синдромального, как медикаментозного так и немедикаментозного лечения после проведения дифференциальной диагностики может дать положительный эффект (например, миорелаксанты, нестероидные противовоспалительные препараты при вертеброгенных поражениях, препараты с антидепрессантной действием, психотерапия при проявлениях депрессии и т.д. ). Важное значение имеет комплексное лечение с применением физиотерапии, рефлексотерапии, кинезотерапии. Больному предлагают постоянно заниматься лечебной физкультурой, вести здоровый образ жизни и т.д..
2). В случае клинического подтверждения субъективных жалоб пациента семейный врач направляет больного второе звено медицинской помощи – к невропатологу, где проводится углубленная дифференциальная диагностика, разрабатывается дальнейшая тактика ведения больного ( с чем должен быть ознакомлен семейный врач) и может быть назначено специфическое лечение. Неспецифическое лечение, которое касается нейропротекции, должно назначаться уже на ранних стадиях паркинсонизма.
Специфическое лечение имеет большое значение в прогнозе заболевания и жизни! Учитывая то, что БП является постепенно прогрессирующим заболеванием, к внедрению препаратов леводопы оно приводило к гибели пациентов в среднем через 10–12 лет от бронхопневмонии и других осложнений, присущих обездвиженным больным. Благодаря этому срок жизни и структура смертности пациентов с БП, существенно не отличаются от таковых в общей популяции. Зато, при наличии деменции отмечается сокращение сроков жизни у больных БП. Следует знать, что медикаментозная терапия при паркинсонизме является пожизненной и постоянной. Перерыв в лечении не повышает эффективности следующей терапии, а на поздних стадиях заболевания может приводить к тяжелому, иногда необратимый ухудшение состояния. Поэтому проводить « лекарственные каникулы » можно только для преодоления тяжелых побочных эффектов (чаще психических расстройств) в стационарных условиях.
На начальных стадиях заболевания допустимо умеренное снижение дозы противопаркинсонических препаратов в дни, когда пациент нуждается в меньшем финкциональнои активности ( выходные, отпуск).
Направления больного третичную звено медицинской помощи в специализированные научно – исследовательские учреждения в сложных или атипичных случаях осуществляется врачом – невропатологом.
3). Врач общей практики контролирует выполнение больным назначений невропатолога и проводит профилактику и лечение сопутствующих заболеваний, которые могут углублять проявления паркинсонизма.
Следует знать, что специфическое лечение паркинсонизма может иметь существенные побочные эффекты, которые вызывают необходимость проведения дифференциальной диагностики – выявление синдромов, вызванных определенным заболеванием или применением фармпрепарата.
Следовательно, важно знать, что деменция может проявляться или увеличиваться при приеме антихолинергических средств или в случае сопутствующей депрессии.
Нарушение сна может быть связано также с препаратами леводопы, если больной их принимает менее чем за 30 минут до отхода ко сну. Длительный прием препаратов леводопы может быть причиной ярких сновидений. Последнее может предшествовать развитию дофаминового психоза. Жалобы больного на плохой сон и раннее утреннее пробуждение могут быть проявлением депрессии.
При длительном лечении препаратами леводопы или агонистами дофаминовых рецепторов в 10–30 % больных развивается спутанность сознания, иллюзии и галлюцинации. Предполагается, что в основе этих расстройств лежит гиперчувствительность лимбических постсинаптических дофаминовых рецепторов противопаркинсонических препаратов, возникает вследствие уменьшения центральной дофаминергических активности. Вероятность развития психоза тем больше, чем больше длительность болезни и лечения. Факторами риска для развития спутанности и « поздних галлюцинаций » на прогрессирующих стадиях является сопутствующая деменция и при – Йом антихолинергических препаратов.
Сначала у больных возникают зрительные иллюзии или псевдогаллюцинации (т.е. больной сохраняет критику к галлюцинациям ), а впоследствии могут появиться истинные галлюцинации ( с отсутствием критики) или паранояльный психоз. Психотические эпизоды иногда возникают также после оперативного вмешательства под местной анестезией или общим наркозом.
В связи с этим семейный врач должен владеть информацией или иметь к ней доступ по побочных осложнений противопаркинсонических препаратов, и в случае их наличия направить больного к невропатологу для просмотра назначений.
4). Врач общей практики должен работать с семьей больного. Нужно проводить разъяснительную беседу с членами семьи относительно особенностей течения патологии. В частности, в наличии у больного невротических, мнестических, эмоциональных, двигательных проявлений следует проявлять терпение со стороны членов семьи, ведь это проявления болезни, а не прихоти – капризы пациента. Болезнь может усугублять некоторые негативные личностные характеристики пациента.
Члены семьи должны контролировать выполнение больным назначений врача, помогать ему в быту.
Только комплекс усилий со стороны врачей, пациента и членов семьи и общества способствовать торможению прогрессирования патологии и повышению качества жизни больного человека.
Ольга КОВАЛЕНКО
д.м.н. , профессор кафедры неврологии и рефлексотерапии НМАПО им . П.Л.Шупика
Наталья ОВОДЮК
врач–невролог ГНУ «НПЦ ПКМ» ГУД , г. Киев